9 月 19 日,NMPA 官网显示,信达生物胰高血糖素(GCG)/胰高血糖素样肽-1(GLP-1)双受体激动剂「玛仕度肽」(IBI362)又一项适应症获批上市,治疗 2 型糖尿病(受理号:CXHS2400070/1/2)。
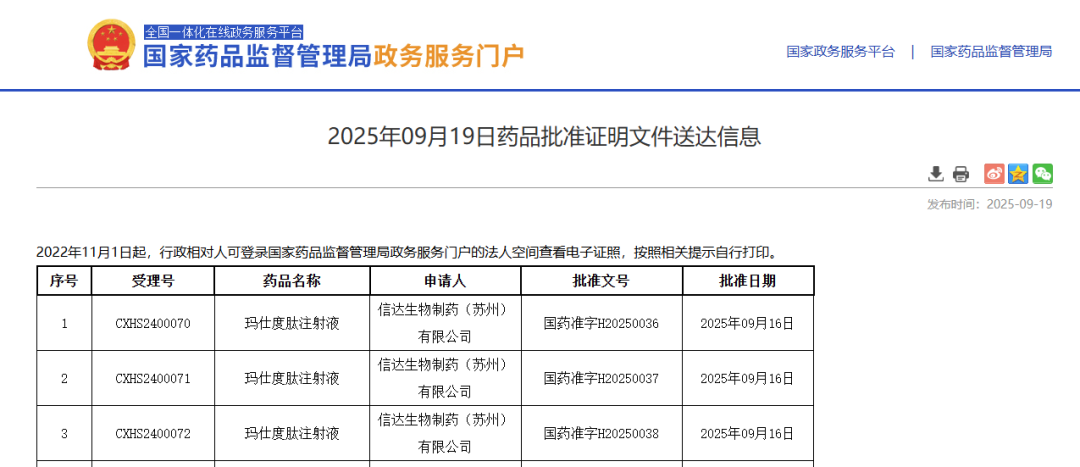
图片来源:NMPA 官网
玛仕度肽是信达生物与礼来制药共同开发的一款 GLP-1R/GCGR 双重激动剂。作为一种哺乳动物胃泌酸调节素(OXM)类似物,玛仕度肽除了通过激动 GLP-1R 促进胰岛素分泌、降低血糖和减轻体重外,还可通过激动 GCGR 增加能量消耗增强减重疗效,同时改善肝脏脂肪代谢,带来多重代谢获益。
2025 年 6 月 27 日,玛仕度肽首次在国内获批上市(点击查看丁香园往期内容:全球首款!这个药刚刚国内获批,或将改写指南),成为全球首个且唯一获批的 GCG/GLP-1 双受体激动减重药物。
首批适应症为:用于在控制饮食和增加体力活动基础上对成人患者的长期体重控制,包括肥胖(初始 BMI ≥ 28 kg/m2)或超重(BMI≥24 kg/m2)并伴有至少一种体重相关的合并症的患者(例如高血糖、高血压、血脂异常、脂肪肝、阻塞性睡眠呼吸暂停综合征等)。
而本次糖尿病适应症的获批,意味着信达成功拿下 GLP-1 类药物的两大核心适应症。
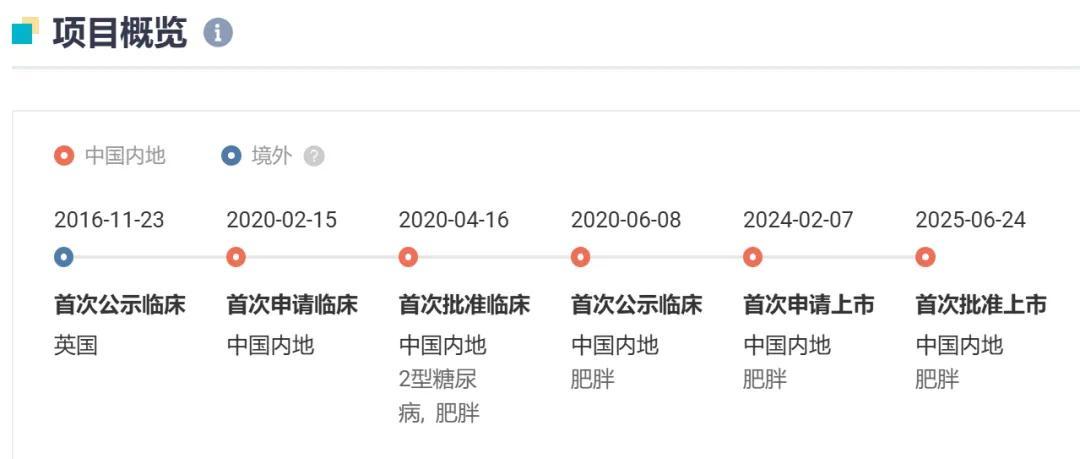
图片来源:丁香园 Insight 数据库网页版
本次获批是基于两项关键 III 期临床研究 DREAMS-1 和 DREAMS-2 的积极结果。
DREAMS-1(NCT05628311/CTR20222875)是一项多中心、随机、双盲、安慰剂对照的 III 期临床研究,在单纯饮食运动控制不佳的中国 2 型糖尿病患者中评估玛仕度肽的有效性和安全性。该研究共纳入了 320 例受试者,研究的主要终点是第 24 周时 HbA1c 较基线的变化。
2025 年美国糖尿病协会(ADA)科学会议最新公布的结果显示,第 24 周时,玛仕度肽组在 HbA1c 水平较基线的平均变化方面显著优于安慰剂组(LSM 治疗差异:玛仕度肽 4 mg 组为 −1.43%;玛仕度肽 6 mg 组为 −2.02%)。
在达到 HbA1c 水平 <7.0%、体重降幅 ≥5%的患者比例,以及同时达到 HbA1c 水平 <7.0% 且体重降幅 ≥5% 的患者比例,以及第 24 周体重较基线的平均百分比变化等各个指标上,玛仕度肽均显著优于安慰剂。
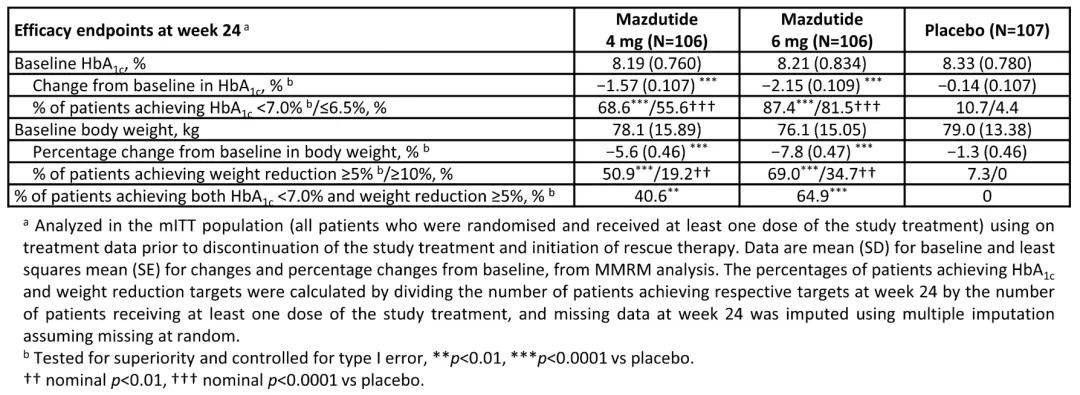
图片来源:ADA 官网
DREAMS-2(NCT05606913/CTR20222740)是一项为期 28 周的随机、开放 III 期临床研究,在既往接受二甲双胍联合或不联合 SGLT-2 抑制剂或磺酰脲类药物血糖控制不佳的中国成人 T2DM 患者中,评估玛仕度肽相对于度拉糖肽的疗效和安全性。该研究共纳入 731 例 T2DM 患者,主要终点为第 28 周时玛仕度肽 4mg 和 6mg 组与度拉糖肽 1.5mg 组相比 HbA1c 相对于基线的变化。
2024 年第 60 届欧洲糖尿病研究协会(EASD)年会上公布的结果显示,基于疗效估计目标,第 28 周时,玛仕度肽 4mg 组和 6mg 组 HbA1c 较基线平均降幅分别为 1.69% 和 1.73%,均优效于度拉糖肽 1.5mg 组(1.38%)(P 值均<0.01);空腹血糖(FPG)水平较基线平均分别降低 2.03mmol/L 和 2.19mmol/L,均优效于度拉糖肽 1.5mg 组(1.71mmol/L)(P 值均<0.05)。
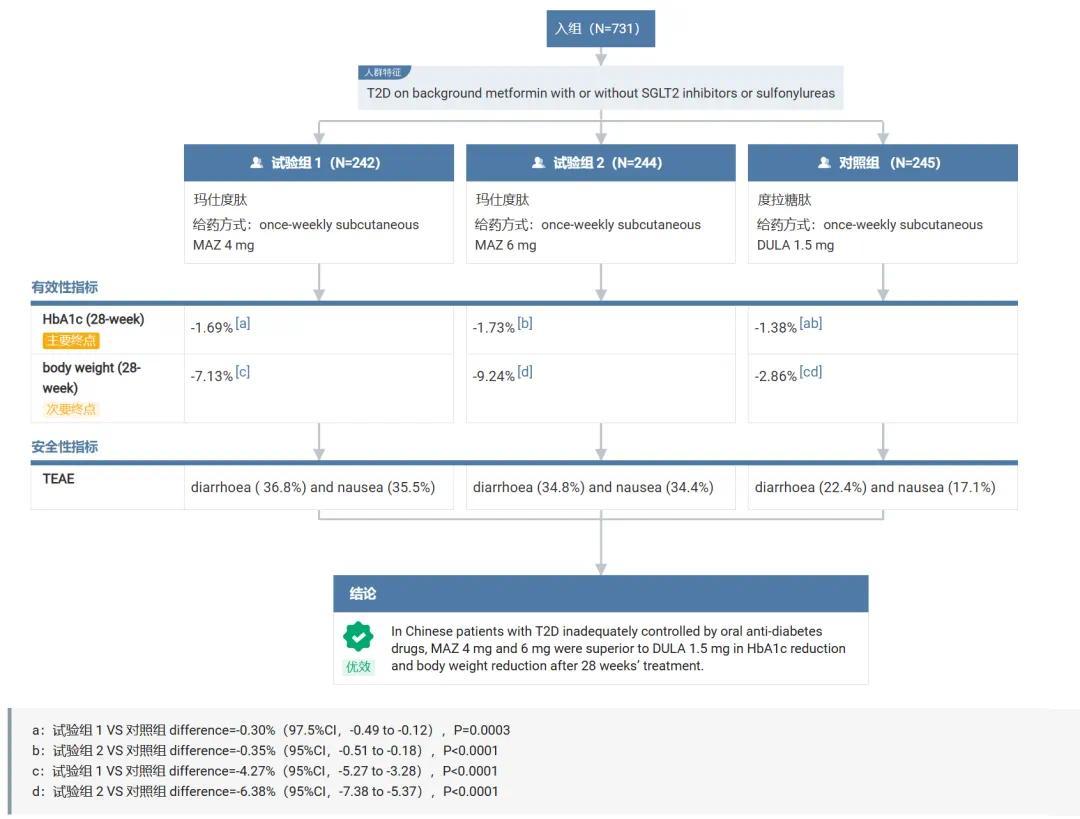
DREAMS-2 临床试验结果,图片来源:丁香园 Insight 数据库
在糖尿病适应症上,信达还启动了第 3 项关键 III 期临床研究 DREAMS-3(NCT06184568/CTR20234187)。
试验拟纳入 342 位受试者,研究主要终点为第 40 周 HbA1c<7.0% 且体重较基线下降 ≥10% 的受试者比例。目前,其临床结果尚未公布。
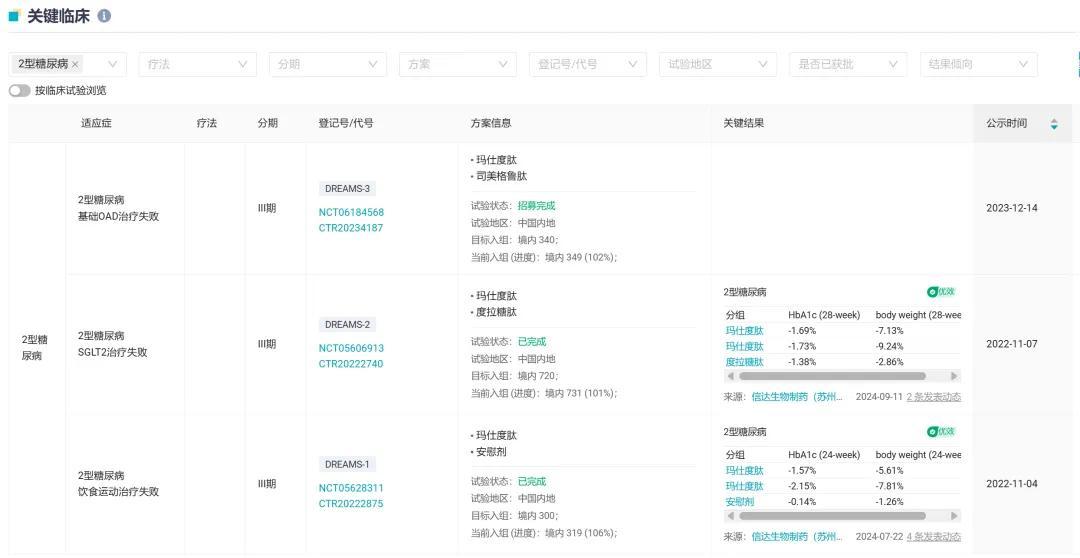
「玛仕度肽」布局的 3 项糖尿病 III 期临床
除肥胖症和糖尿病之外,还布局了中至重度阻塞型睡眠呼吸暂停(OSA)、代谢功能障碍相关脂肪性肝病(MAFLD),均已启动 III 期临床。
已开展的 III 期临床研究具体如下:
在中国超重或肥胖受试者中开展的 GLORY-1
在中国中重度肥胖受试者中开展的 GLORY-2
在中国超重或肥胖合并 MAFLD 受试者中开展的对比玛仕度肽和司美格鲁肽的 GLORY-3
在初治的中国 2 型糖尿病受试者中开展的 DREAMS-1
在口服药物治疗血糖控制不佳的中国 2 型糖尿病受试者中开展的对比玛仕度肽和度拉糖肽的 DREAMS-2
在中国 2 型糖尿病合并肥胖的受试者中开展的对比玛仕度肽和司美格鲁肽的 DREAMS-3
在中国阻塞性睡眠呼吸暂停合并肥胖患者中开展的 GLORY-OSA
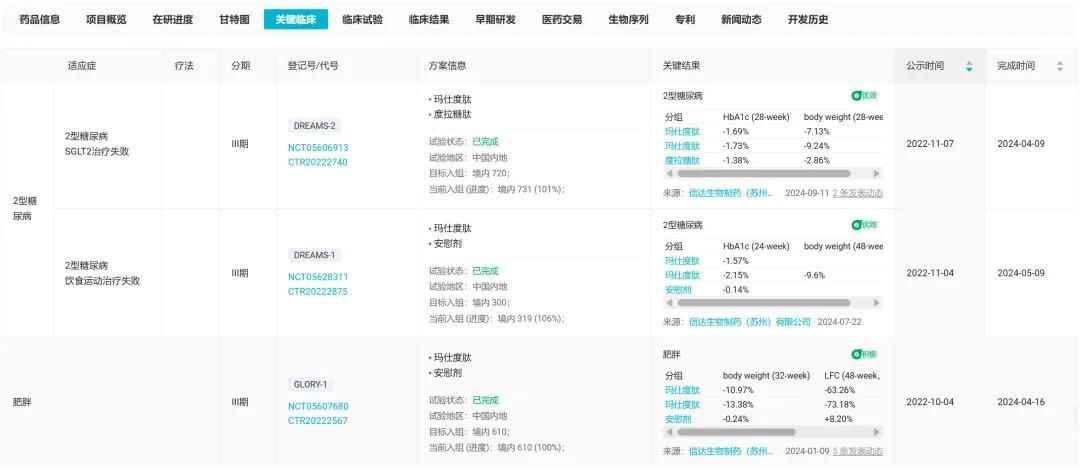
已公布 III 期临床结果,图片来自:丁香园 Insight 数据库
除此之外,信达也布局了心力衰竭适应症。2025 年 2 月 18 日,信达首次登记公示了玛仕度肽在射血分数保持的心力衰竭(HFpEF)或射血分数轻度降低的心力衰竭(HFmrEF)合并肥胖的中国成人患者中的 II 期临床试验(NCT06862908/CTR20250152),如今正在进行中。
编辑:ccai
编辑:ccai
