本文作者:哈基鼠你这家伙……
一年畅销 163 亿的药物,获批时饱受争议,又因增加死亡风险被黑框警告,
而最近,它再度提交了新适应症申请。这一次,如果能够获批,它将成为该领域近 30 年来首款新药。

FDA 文件截图
年销 163 亿,最畅销的精神类药物之一
这个争议重重的药物,名为布瑞哌唑。
上周五,FDA 精神药物咨询委员会(PDAC)召开会议,就布瑞哌唑是否可以作为创伤后应激障碍(PTSD)患者的起始治疗方案进行了讨论与投票。
布瑞哌唑(Brexpiprazole)是一种非典型抗精神病药物,能够同时调节神经传统系统的多个靶点,既包括了部分激动多巴胺 D2 受体和 5-HT1A 受体、也可拮抗 5-HT2A 受体拮抗。
布瑞哌唑的分子式
由于多靶点作用机制的复杂性,布瑞哌唑被认为有可能起到改善精神分裂症状、抗焦虑、抗抑郁、改善认知功能、镇定的潜在效果。
2015 年 7 月,布瑞哌唑首次获得美国 FDA 批准,用于成人重度抑郁症的辅助治疗以及成人精神分裂症。随后,又先后获批用于 13~17 岁的青少年精神分裂症、阿尔茨海默病激越。
仅 2023 年,布瑞哌唑就卖出 22.72 亿美元(约合人民币 163 亿),是全球最畅销的精神治疗药物之一。
而这一次,布瑞哌唑剑指的是精神科的「老大难」——创伤后应激障碍(PTSD)。
在精神科疾病中,PTSD 是严重缺乏有效治疗的典型代表。
截至目前,仅有舍曲林(Zoloft)和帕罗西汀(Paxil)两种选择性 5-羟色胺再摄取抑制剂(SSRI)获批用于 PTSD,但是有研究显示,约有 40~60% 的 PTSD 患者对药物治疗没有反应[1]。
有问题,就有机遇。作为拥有多靶点的新一代抗精神病药物,布瑞哌唑很早就开始布局 PTSD 适应症,临床试验最早可以追溯回 2017 年。
去年 4 月,布瑞哌唑提交补充新药申请,申请联合舍曲林用于成人 PTSD。如果能够顺利获批上市,它将成为 PTSD 领域近 30 年来的首款新药。
故事讲到这里,听上去前途一片光明。但不巧,布瑞哌唑端上来的,是两份自相矛盾的临床 3 期结果。
两项 3 期互相矛盾,FDA 投票 10:1 不支持
本次 FDA 开会重点讨论的,是布瑞哌唑的两项随机、双盲、主动对照 3 期试验 Trail 071 和 Trail 072。
两项研究试验组均为布瑞哌唑+舍曲林,对照组则为舍曲林+安慰剂。不同之处在于:
Trail071 采用了灵活剂量调整的方案,也就是根据对患者临床症状的评估采用 2mg 或 3mg 的布瑞哌唑和固定剂量的舍曲林,比较与舍曲林单药的疗效差异。
Trail072 则采用了固定剂量,不同组别的患者始终保持 2mg 或 3mg 布瑞哌唑联用舍曲林的药物治疗方案。
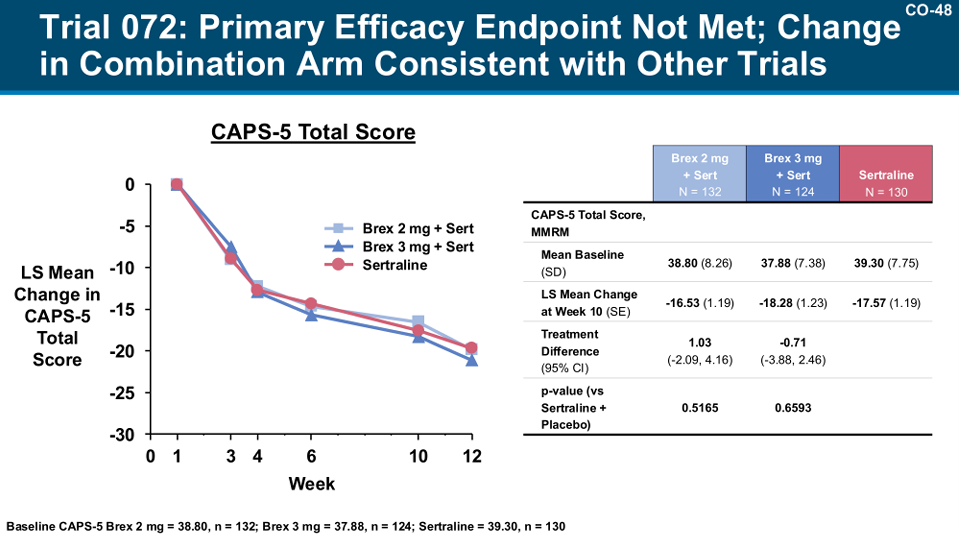
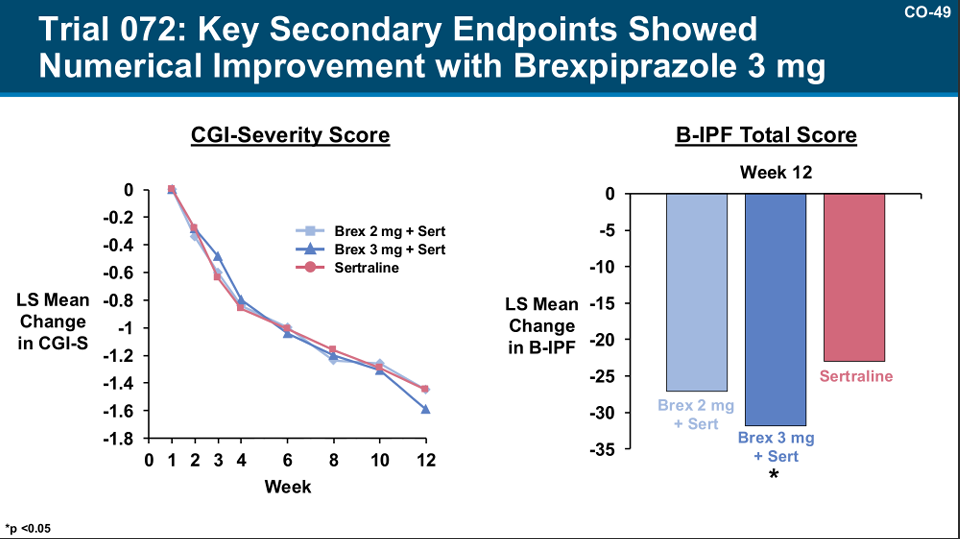
研究截图
奇怪的是,Trail071 结果显示,布瑞哌唑与曲舍林联用有效,显著改善了患者的 PTSD 症状;但在 Trail072 中,无论使用 2mg 还是 3mg 的布瑞哌唑,症状改善与对照组之间差异均不达统计学显著,甚至两个剂量组之间也基本没差别。
两项 3 期结果,互相矛盾了。
另一方面,在 Trail 071 中,布瑞哌唑+曲舍林的不良事件停药率仅 3.9%,显著低于安慰剂+舍曲林组的 10.2%。
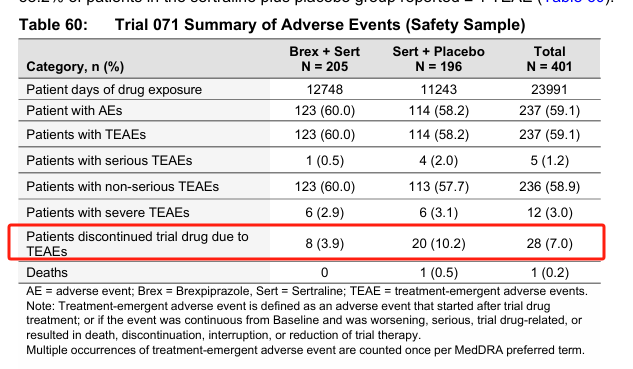
研究截图
几种可能的解释是,布瑞哌唑副作用强烈,实验组患者能够识别出自己吃的并非安慰剂,因此不愿轻易停药。也有可能是舍曲林+安慰剂组效果不如预期,导致患者主观感觉「无效」而停药。
但无论如何,考虑到一款新药通常需要有两项阳性的确证性 3 期临床试验来支持上市申请,布瑞哌唑不出意料地被 FDA 指控没有充分的 PTSD 疗效证据。
对此,布瑞哌唑补充提交了的 2 期临床试验 Trial 061 来验证药物的有效性。
Trial 061 中,患者被分为 4 组,分别是布瑞哌唑(1~3mg/天)+舍曲林(100~200mg/天)、布瑞哌唑+安慰剂、舍曲林+安慰剂、安慰剂+安慰剂。结果发现,布瑞哌唑+舍曲林的症状改善,要显著优于舍曲林+安慰剂。
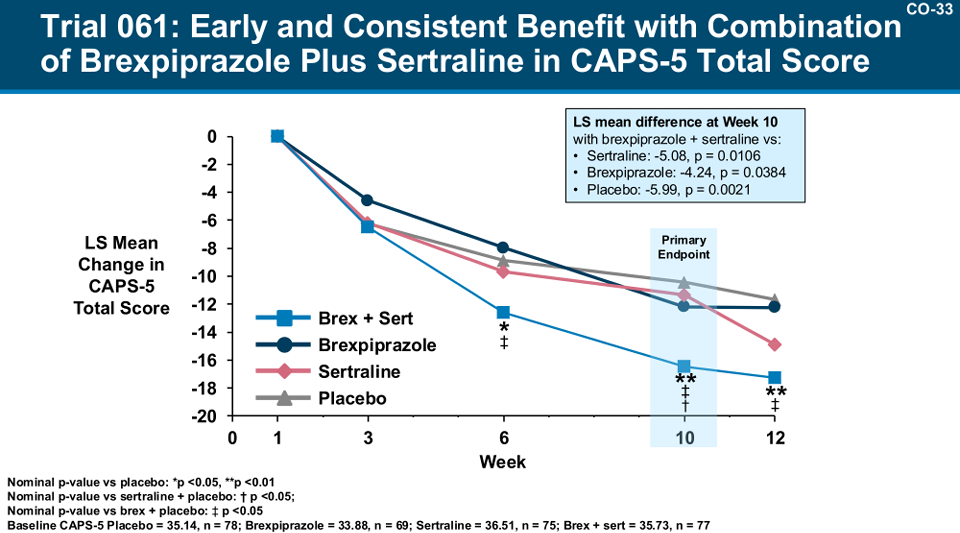
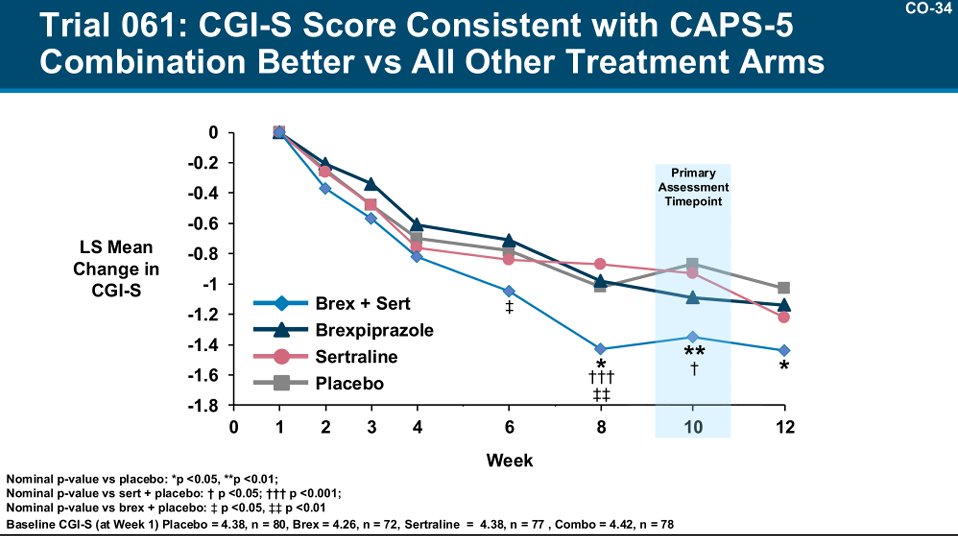
研究截图
然而,这份研究也有瑕疵,舍曲林这个在 PTSD 领域用了近 30 年的药,做出来的效果居然跟纯安慰剂组差异不显著……不出意料,FDA 认为 Trial 061 应该被视为一个存在局限性的探索性试验,用来寻求获批是不适宜的。
最终,FDA 精神药物咨询委员会(PDAC)以 10-1 的高票,不建议批准「布瑞哌唑+舍曲林用于 PTSD 治疗」。

PDAC 投票结果
尽管专家咨询委员会的投票并不直接决定最终审批结果,但 FDA 在进行审批时,会着重考虑专家咨询委员会的意见,大多数情况下,会做出与专家咨询委员会相一致的决定。
但需要强调的是,咨询委员会的投票并不代表着布瑞哌唑完全无效,而是认为当前临床试验证据不充分,后续 FDA 也很有可能要求布瑞哌唑补充更多临床试验数据,再重新提交上市申请。
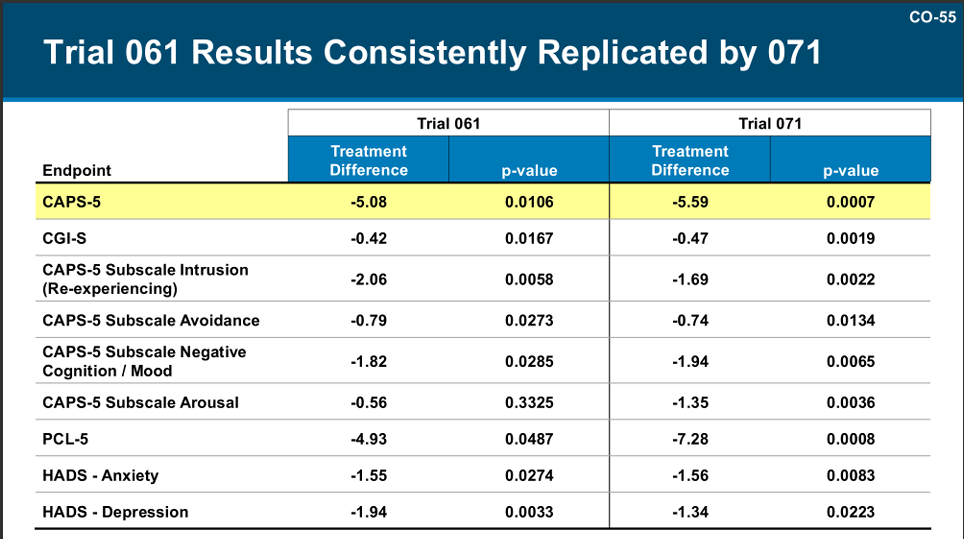
研究截图
争议缠身:增加死亡风险,仍然获批上市
「30 年来首款 PTSD 新药」的不确定性增加了,但对于布瑞哌唑来说,这也并非第一次受到争议。
布瑞哌唑之所以有着现在的名气与关注度,很大程度上与其获批阿尔茨海默病激越(Agitation in Alzheimer’s disease,AAD)的过往相关。
2023 年 5 月,布瑞哌唑在美国获批用于治疗 AAD,随即引发了广泛的讨论与批评。

FDA 截图
其中最重要的争议点在于,布瑞哌唑会增加 AD 患者死亡风险。
AD 的概念我们已经不陌生,「激越」则是指痴呆或 AD 患者中最常见的一种行为和心理症状,表现包括情绪不安(如焦虑、紧张、烦躁),过度行为(如徘徊、坐立不安),言语或肢体攻击性(如大声喊叫、辱骂、推打)。
「激越」通常出现在疾病中后期或严重认知退化阶段,患者伤人的可能性上升,也显著增加看护和医疗的成本。
为寻求 AAD 适应症获批,布瑞哌唑连做了三个 3 期临床试验:灵活给药的 Trial 284 中布瑞哌唑与安慰剂组无疗效差异;固定剂量的 Trial 283 中,只有 2mg 剂量组展现出了与安慰剂组的差异,但仅仅有科恩-曼斯菲尔德激越量表(CMAI)量表上 3.8 分的评分改善。
直至 Trail213,布瑞哌唑才见到了一点曙光:与安慰剂相比,治疗 12 周后,布瑞哌唑可减轻 5.3 分的症状,尽管远低于 17 分的阈值,但也能勉强证明其存在一定疗效。
医学顶刊 BMJ 在当时的报道中,将这一结果描述为「并不显著的疗效」。
BMJ 截图
与疗效勉强相对的,是显著的死亡风险。
在三项 3 期临床试验中,共报告了 9 例死亡患者(Trial 283 中 1 例;Trial 284 中 1 例;Trail213 中试验组 6 例,安慰剂组 1 例),其中 8 例来自布瑞哌唑组。
不过,这一次,FDA 专家会议却以 9:1 的高票同意了「布瑞哌唑的获益大于风险」。在一片争议声中,布瑞哌唑正式获批 AAD 适应症。
在无药可医的困境下
尽管备受争议,但实际上,这并非是一次毫无根据的获批。
一方面,虽然布瑞哌唑组出现 8 例死亡,但患者死因复杂,多为心血管或感染原因,考虑到 AD 患者的身体情况普遍比较差,不能完全说明是由药物导致的患者死亡。
因此,FDA 认为,布瑞哌唑的死亡风险「似乎与其他抗精神病药物对老年痴呆患者的已知风险一致」,同时,还在产品标签上保留了有关死亡风险的醒目黑框警告。
另一方面,同样源于 AAD 的临床诊疗困境。
「AD 发展到一定阶段,可能会出现比较严重的精神行为异常,比如被窃妄想、被害妄想、囤积癖、攻击行为等,对于照护者的压力是很大的。」中国老年保健协会阿尔茨海默病分会(ADC)常务副主任委员兼秘书长、北京大学第一医院主任医师孙永安教授这样说。

孙永安教授是《中国阿尔茨海默病痴呆诊疗指南》的作者之一,他指出,截至目前还没有一款专门针对 AD 精神行为异常的药物。而一些常见的精神药物,如奥氮平、喹硫平等,药品说明书中明确指出「不批准用于痴呆相关的精神病患者」。
FDA 自 2005 年起针对非典型抗精神病药物发布黑框警告,2008 年进一步扩展至所有典型及非典型抗精神病药,强调「AD 相关精神病患者使用抗精神病药物死亡风险显著升高」。[2]

JAMA 相关论文截图
「在这样的背景下,当有家属强烈要求治疗这一类的症状时,也会有医生在充分沟通后,结合患者的精神行为异常,从很小的剂量谨慎地用起。」孙永安教授说。
「但这种违规用药,医疗风险是很高的。」孙永安教授认为,布瑞哌唑的出现解决了两个很大的问题。「一方面是 AD 的异常精神症状有药可治;另一方面,这种治疗在药物适应症范围之内,也能受到法律的保护。」
在关于布瑞哌唑获批 AAD 的争论中,同样有支持者指出,不批准并不意味着患者不会使用,相反,获批意味着意味着有经过验证的剂量和监测方案,反而提高了用药安全可控性。
但也有反对者认为,这种药物存在被滥用的可能。
有调查报道指出[5],由于养老院护工的人手不够,以 2019 年的养老院护工配置水平估算,可能约有 24000 名美国养老院住户接受了不必要的镇静剂,以实现「化学约束」——相似的情况,也有可能出现在布瑞哌唑中。
需要指出的是,截至目前,布瑞哌唑在中国获批上市的适应症仅包含成人精神分裂症。而这款药物的核心化合物专利将于 2026 年 4 月到期,已有十余家中国药企布局布瑞哌唑的仿制和改良药项目。(策划:z_popeye|监制:islay)
题图来源:图虫创意
参考资料:
[1]https://pmc.ncbi.nlm.nih.gov/articles/PMC3278188/
[2]https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2765053?utm_source=chatgpt.com
[3]How the FDA approved an antipsychotic that failed to show a meaningful benefit but raised the risk of death BMJ 2023; 382 doi: https://doi.org/10.1136/bmj.p1801 (Published 17 August 2023)
[4]De Mauleon A, Ismail Z, Rosenberg P, et al. Agitation in Alzheimer’s disease: Novel outcome measures reflecting the International Psychogeriatric Association (IPA) agitation criteria. Alzheimers Dement2021;17:1687-97. doi:10.1002/alz.12335. pmid:34132461
[5]https://www.marketwatch.com/story/nursing-homes-may-start-sedating-your-elderly-parents-and-eventually-you-because-they-dont-have-enough-workers-e4c47a89?mod=brett-arends
编辑:ifhealth 来源:丁香园
